齊魯網·閃電新聞12月21日訊 山東省藥品監督管理局日前發布今年第3期藥品質量抽檢通告,通告顯示,山東命大藥業有限公司、北京鶴延齡藥業發展有限公司、成都天臺山制藥有限公司、陽信縣人民醫院等生產、銷售或使用的4批次藥品不符合標準規定。

為加強藥品質量監管,保障公眾用藥安全,依據省藥監局年度抽檢工作計劃,省局對藥品生產、經營、使用單位進行了藥品質量抽查檢驗,現將抽檢發現的不符合規定的藥品情況通告如下:
經核查確認,標示4家生產企業的4個品種共4批次藥品,經抽檢不符合標準規定。
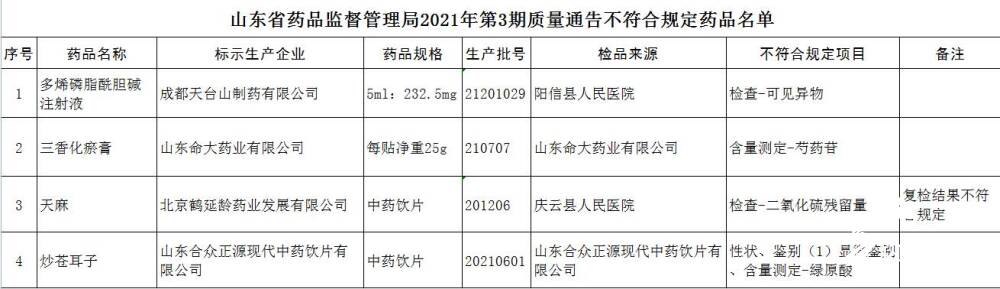
具體不合格情況如下:
來自陽信縣人民醫院的標示成都天臺山制藥有限公司生產的多烯磷脂酰膽堿注射液不符合標準規定。
來自山東命大藥業有限公司的三香化瘀膏不符合標準規定。
來自慶云縣人民醫院的標示北京鶴延齡藥業發展有限公司生產的天麻不符合標準規定。
來自山東合眾正源現代中藥飲片有限公司的炒蒼耳子不符合標準規定。
相關藥品監管部門對不符合規定產品已采取查封、扣押、暫停銷售、產品召回等控制措施,并依據相關法律法規對有關生產企業(配制單位)、被抽樣單位依法嚴肅查處,查處情況可查詢山東省藥品監督管理局或相關市市場監督管理局網站。
對不符合規定產品及相應生產經營企業、單位,相關藥品監管部門要加強監管,督促其查明問題原因,制定落實整改措施,切實消除風險隱患。
閃電新聞記者 何則偉 報道



























